Die Wahl eines Herstellers von Pharmamaschinen klingt einfach: Spezifikationen vergleichen, Angebote einholen, sich für einen bekannten Namen entscheiden. In der Praxis zeigen sich die meisten Probleme jedoch erst später: verpasste Liefertermine, mangelhafte Dokumentation, langsamer Service und vermeintlich kleine Konstruktionslücken, die sich zu großen Validierungs- und Verfügbarkeitsproblemen ausweiten. Dieser Leitfaden hilft Ihnen, den optimalen Partner für Ihre Bedürfnisse zu finden – egal, ob Sie neu im Bereich Pharmaanlagen sind oder bereits Erfahrung haben und einfach weniger Überraschungen erleben möchten.
Wir stellen Ihnen 10 sinnvolle Prüfpunkte vor, mit denen Sie jeden Anbieter von Pharmamaschinen vergleichen können. Hersteller von pharmazeutischen Anlagen —von der ersten Vorauswahl bis hin zu FAT/SAT und langfristiger Unterstützung. Zunächst benötigen Sie jedoch etwas, das viele Teams vernachlässigen.

Für einen aussagekräftigen Vergleich ist ein klar definierter Untersuchungsgegenstand unerlässlich. Andernfalls erscheint jeder Anbieter auf dem Papier gut, weil die Fragestellung nicht einheitlich und präzise formuliert ist.
Betrachten Sie diesen Schritt als die Umwandlung einer vagen Idee („Wir brauchen eine Leitung“) in eine einfache, kundenfreundliche URS (User Requirement Specification). Sie muss weder formell noch abschreckend sein – nur so präzise, dass zwei Hersteller vergleichbare Antworten geben.
●
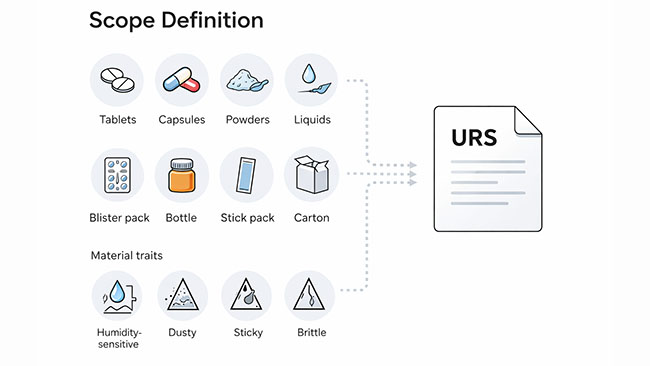
Produkt- und Prozessrealität
Darreichungsform (
Tabletten
, Kapseln, Pulver, Granulat, Pellets, Flüssigkeiten), Verpackungsformat (
Blisterverpackungen
, Flaschen, Stickpacks/Beutel, Kartons), sowie Materialeigenschaften (feuchtigkeitsempfindlich, staubig, klebrig, spröde).
●
Ausgabe- und Chargenrhythmus
Zielvorgaben für Packungen pro Stunde, Schichtmuster, Chargengrößen und die Häufigkeit von Formatwechseln. Hohe Geschwindigkeit nützt nichts, wenn Umrüstungen den ganzen Tag in Anspruch nehmen.
●
Ziel für Qualität und Konformität
Wo das Produkt verkauft wird und welche Standards (cGMP/GMP-Anforderungen, Dokumentationsumfang, Datenanforderungen) eingehalten werden müssen, beeinflusst unmittelbar die Leistungen des Herstellers – nicht nur die der Maschine.
●
Einschränkungen der Einrichtung
Grundfläche, Deckenhöhe, Zugangswege, Versorgungsleitungen (Strom, Druckluft, Vakuum, Kühlung) und Reinheitsanforderungen. Das sind häufige Ausschlusskriterien.
●
Automatisierungsgrad und Personalplanung
Wünschen Sie sich eine „bedienerfreundliche Lösung mit Schutzmechanismen“ oder eine „von Ingenieuren optimierte Leistung“? Wer wird das Gerät im täglichen Betrieb bedienen und wie sicher ist diese Person in der Fehlerbehebung?
●
Zeitplan und Integration
Gewünschter Liefertermin, Installationszeitraum und ob eine Integration mit vorgelagerten/nachgelagerten Anlagen erforderlich ist (z. B. Blisterverpackung → Kartonierung oder Zählung → Verschließen → Etikettierung).
|
von Ihnen definierter Bereichseingang |
Was sich im Angebot und im Design ändert |
|
Darreichungsform + Packungsformat |
Maschinentyp, Werkzeuge, Dichtungsverfahren, Umrüstteile |
|
Zielausgabe + Chargengrößen |
Dimensionierung des Antriebssystems, Puffer, Auswurflogik, OEE-Erwartungen |
|
Anforderungen an die Einhaltung von Vorschriften/Dokumentation |
IQ/OQ-Bereitschaft, Rückverfolgbarkeit, Testprotokolle, Softwarefunktionen |
|
Anlagengrenzen (Platz/Versorgungseinrichtungen) |
Layout, Schutzvorrichtungen, Staubkontrolle, Strom-/Luftspezifikationen |
|
Umschaltfrequenz |
Schnellwechseldesign, Werkzeugstrategie, Trainingsintensität |
|
Integrationsbedarf |
Liniensteuerung, Handschlag, Förderbänder, Verantwortungsgrenzen |
Bevor Sie mit dem Vergleich der Hersteller beginnen, stellen Sie sicher, dass Sie diese Fragen in einfachen Worten beantworten können:
● Welches Produkt bieten wir an und in welcher Verpackungsform versenden wir es?
● Was ist das angestrebte Ergebnis und wie groß ist die typische Batchgröße?
● Welche Qualitätskontrollen und Ausschlusskriterien sind unbedingt erforderlich?
● Welche Dokumentation benötigen wir bei der Übergabe (Basisdokumentation vs. Validierungsdokumentation)?
● Welcher Platz und welche Versorgungsanschlüsse stehen zur Verfügung?
● Wie oft werden wir die Formate ändern und wie schnell müssen wir diese Änderungen vornehmen?
● An welche Geräte muss dieses Gerät (stromaufwärts/stromabwärts) angeschlossen werden, falls überhaupt?
Wenn Sie vor der Angebotsanfrage nur eine Sache tun, dann diese. Dadurch wird der restliche Prozess der Auswahl eines Herstellers von Pharmamaschinen schneller, objektiver und es wird für schwache Anbieter deutlich schwieriger, sich hinter vagen Versprechungen zu verstecken.
Als nächstes nutzen wir Ihren Umfang, um eine Auswahlliste zu erstellen, die tatsächlich vergleichbar ist – damit Sie nicht Äpfel mit Birnen vergleichen.
Sobald Ihr Projektumfang klar definiert ist, sollten Sie als Nächstes sicherstellen, dass Sie die Hersteller von Pharmamaschinen unter vergleichbaren Bedingungen vergleichen. Hier verlieren viele Einkäufer Zeit: Sie holen 6–10 Angebote ein, die nicht einmal die gleichen Leistungen beschreiben.
Hier ist eine einfache Möglichkeit, eine Vorauswahl an Herstellern von pharmazeutischen Maschinen zu treffen, ohne sich in Marketingversprechen zu verlieren:
Beginnen Sie mit 6 „Nachweisartikeln“ für jeden Lieferanten
● Ähnliche Projekte: gleiche Darreichungsform + ähnliches Ergebnis + ähnliches Verpackungsformat.
● Klare Abgrenzung des Leistungsumfangs: Was ist enthalten (Maschine, Werkzeuge, Förderbänder, Versorgungseinrichtungen, Installation, Schulung, Ersatzteile)?
● Dokumentationsbeispiele: Beispielhaftes FAT-Protokoll, Handbücher, Teilelisten und (falls erforderlich) IQ/OQ-Vorlagen.
● Serviceabdeckung: Reaktionszeit, Verfügbarkeit von Ersatzteilen und ob Fernwartung und Vor-Ort-Service angeboten werden.
● Fabriksignale: Echte Produktionskapazität (nicht nur ein Büro). Fragen Sie nach Fotos/Videos aus der Produktionshalle und einem einfachen Besichtigungsprogramm.
● Benannte Referenzen: mindestens 1–2 Kunden, mit denen Sie sprechen können (auch wenn diese anonymisiert sind, können Sie die Geschichte dennoch überprüfen).
Warnsignale, die später in der Regel Geld kosten
● Aussagen, die konkrete Details vermeiden: „hohe Qualität“, „fortschrittlich“, „anpassbar“, aber keine Testmethode, keine Toleranz, keine Akzeptanzkriterien.
● „Alles ist inklusive“ – ohne Auflistung der Leistungen.
● Kein klarer Plan für FAT/SAT, die Übergabe der Dokumentation oder das Änderungsmanagement.
● Vage Serviceversprechen: „Lebenslanger Support“ ohne Angabe von Reaktionszeit oder Ersatzteilplan.
Ein kurzer Realitätscheck: Erfolgreiche Hersteller sprechen in der Regel mit Zahlen und Prozessen (Mitarbeiterzahl, F&E-Kapazitäten, Rückverfolgbarkeit, Warenausgangsprüfungen, Reaktionszeiten). Beispielsweise legen etablierte Bauunternehmen offen Details wie eigene F&E-Teams, geprüfte Managementsysteme (ISO + 6S), vollständige Rückverfolgbarkeit der Beschaffung und Vorversandtests wie z. B. Langzeit-Dauerlauf offen. Diese operativen Details helfen Ihnen, echte Leistungsfähigkeit von einer guten Website zu unterscheiden.

„Hersteller von pharmazeutischen Ausrüstungen“ ist eine weit gefasste Bezeichnung. Lieferant für eine Kapselfüllmaschine ist möglicherweise nicht das Beste für ein Hochgeschwindigkeits-Blisterverpackungsmaschine Linienintegration.
Verwenden Sie kategoriespezifische Fragen. Sie brauchen keine 50 davon – nur diejenigen, die echte Erfahrungen aufdecken.
● Welchen Dosierbereich verwenden Sie und wie überprüfen Sie die Abfüllgenauigkeit?
● Wie schnell erfolgt ein tatsächlicher Umrüstvorgang (mit geschulten Bedienern, nicht mit Ingenieuren)?
● Welches Reinigungskonzept wird verfolgt und welche Teile sind für eine schnelle Demontage konzipiert?
● Wie kontrollieren Sie Gewichtsschwankungen und sortieren Tabletten aus, die nicht den Spezifikationen entsprechen?
● Welches Ökosystem für Revolver- und Werkzeugsysteme unterstützen Sie, und wie schnell können Sie Verschleißteile liefern?
● Wie gehen Sie mit Staub um (Entstaubung, Absaugung, Abdichtung)?
● Welches Umformverfahren eignet sich für mein Produkt (Thermoformen vs. Kaltumformen) und warum?
● Wie lassen sich Web-Tracking und Registrierung schnell handhaben?
● Wie gehen Sie bei der Prüfung der Dichtungsintegrität vor (und was bedeutet „bestanden/nicht bestanden“)?
● Zählgenauigkeit und Ablehnungslogik: Wie lässt sich dies während des FAT nachweisen?
● Wie lässt sich ein Produktwechsel ohne lange Ausfallzeiten realisieren?
● Wie geht man mit Staub, statischer Aufladung und empfindlichen Produkten um?
● Welche Kartonreichweite ist nachgewiesen (nicht „möglich“)?
● Optionen für die Blattverarbeitung, Bereitschaft zur Codierung/Serialisierung und Verhalten bei Störungen unter Zeitdruck.
Vor- und Nachteile
● Komplette Produktionslinie von einem einzigen Lieferanten
◆ Vorteile: klarere Verantwortlichkeiten, weniger Schnittstellenkonflikte, einfachere Inbetriebnahme.
◆ Nachteile: Man setzt auf die Kaderbreite eines einzigen Teams über alle Maschinentypen hinweg.
● Erstklassige Maschinen von verschiedenen Anbietern
◆ Vorteile: höhere Spezialisierung pro Maschine.
◆ Nachteile: Das Integrationsrisiko steigt (Kontrollen, Förderanlagen, Zeitplanung, Verantwortlichkeit für Probleme).
Zertifizierungen sind hilfreich, aber was Sie bei echten Audits wirklich schützt, sind Nachweise: schriftliche Verfahren, rückverfolgbare Teile, validierte Funktionen und kontrollierte Dokumentation.
Wenn Sie in die USA exportieren, werden Sie mit den cGMP-Anforderungen der FDA konfrontiert (insbesondere 21 CFR Parts 210 und 211).
US-amerikanische Lebensmittel- und Arzneimittelbehörde
)
Wenn Sie in die EU exportieren, werden Sie den Begriff „EU-GMP“ hören, und für die Qualifizierung/Validierung von Geräten ist Anhang 15 ein gängiger Bezugspunkt.
Öffentliche Gesundheit
)
Dokumente, die man frühzeitig anfordern sollte (damit man ihnen später nicht hinterherlaufen muss).
● Benutzerhandbücher + Wartungshandbücher
● Elektropläne + Pneumatikpläne
● Ersatzteilliste + empfohlene kritische Ersatzteile
● Material- und Teilekennzeichnungen (sofern relevant)
● FAT-Protokollvorlage + Beispiel für Testdatensätze
● Änderungsmanagement / Umgang mit Abweichungen
l Falls Sie Validierungsvorbereitungen benötigen: URS-Mapping, IQ/OQ-Vorlagen, Kalibrierungszertifikate
Wenn es um Software/Daten geht (Alarme, Prüfprotokolle, elektronische Aufzeichnungen)
Fragen Sie direkt nach, ob der Hersteller der pharmazeutischen Maschinen Ihre Erwartungen hinsichtlich elektronischer Aufzeichnungen/E-Signaturen erfüllen kann (oftmals im Rahmen des Anwendungsbereichs von FDA Part 11 behandelt).
Die meisten Projekte erfordern individuelle Anpassungen – Format der Bauteile, Zuführung, Staubabsaugung, Layout, Bedienoberflächen. Die Frage ist, ob diese Anpassungen wie bei einer Konstruktionsplanung oder eher improvisiert werden.
Wie „echte Ingenieurskompetenz“ aussieht
● Sie können einen Designprüfungsprozess (auch informell) aufzeigen.
● Sie können erläutern, was sie nicht anpassen werden, weil es die Stabilität oder Validierung beeinträchtigt.
● Sie können auf frühere Änderungen verweisen und darauf, was sich in der Dokumentation und den Tests geändert hat.
Praktische Fragen
● Wie viele Ingenieure betreuen diese Produktlinie (Mechanik + Elektrotechnik + Steuerungstechnik)?
● Wie lange ist die übliche Lieferzeit für Sonderanfertigungen?
● Wenn während der Entwicklungsphase eine Änderungsanforderung gestellt wird, wie wird diese dokumentiert und bepreist?
(Leichter Richtwert, keine Regel): Wenn ein Lieferant offen über nachhaltige Investitionen in Forschung und Entwicklung sowie über eine entsprechende Anzahl an Ingenieuren sprechen kann, ist das oft ein besseres Zeichen als die Angabe „kundenspezifische Lösungen verfügbar“ in einer Broschüre.
Eine Maschine kann noch so gut gebaut sein und Ihr Projekt dennoch zum Scheitern bringen, wenn der Service langsam oder unklar ist. Behandeln Sie den Service wie einen integralen Bestandteil des Produkts.
Grundlagen des Service zur Verdeutlichung
● Installations- und Inbetriebnahmeumfang (Wer macht was und was müssen Sie bereitstellen?)
● Schulungsplan (Übergabe von Bedienern, Wartungspersonal und Dokumentation)
● Ersatzteilplan (Liste der wichtigsten Ersatzteile, Preise, Versandoptionen)
● Fernsupportprozess (Video-Fehlerbehebung, Reaktionszeit)
● Vorbeugendes Wartungsprogramm und optionaler AMC-ähnlicher Support (jährlicher Wartungsvertrag)
Wenn ein Anbieter mit „schnellem Support“ wirbt, fragen Sie nach konkreten Angaben:
● Zielvorgabe für die Reaktionszeit (Stunden)
● typische Lieferzeit für kritische Ersatzteile
● Eskalationspfad bei Produktionsausfall
Dies ist der Schritt „Vertrauen ist gut, Kontrolle ist besser“ – ohne dabei in einen Papierkram-Overkill zu verfallen.
Referenzprüfungen (halten Sie sie einfach)
● „Was hat Sie nach der Installation überrascht?“
● „Wie sind sie mit dem ersten richtigen Zusammenbruch umgegangen?“
● „Entsprach die Dokumentation Ihren Anforderungen?“
● Würden Sie wieder bei ihnen kaufen?
Werksbesichtigung: Worauf Sie achten sollten
● Einheitlichkeit der Montage (standardisierte Verkabelung, Beschriftung, Sauberkeit, Organisation)
● Denkweise in Bezug auf Wareneingangskontrolle und Rückverfolgbarkeit
● Testkultur: Werden strukturierte Tests durchgeführt oder nur kurze Demos?
FAT/SAT: Frühzeitig nach den Akzeptanzkriterien fragen
Ein solider Werksabnahmetest (FAT) bedeutet nicht einfach nur „das System läuft“. Er bedeutet „das System läuft und beweist die Ergebnisse“. Viele seriöse Lieferanten führen Langzeitläufe durch, da kurze Tests Stabilitätsprobleme verschleiern können. Rich Packing bietet beispielsweise Vorversandtests an, die einen 24-Stunden-Dauerlauf sowie eine zusätzliche Überprüfung unter hoher Last umfassen können. Nutzen Sie dies als Maßstab für den von Ihnen geforderten Nachweis, nicht als bloße Pflichterfüllung.
 Vorlieferungstests der pharmazeutischen Maschinen von Rich Packing
Vorlieferungstests der pharmazeutischen Maschinen von Rich Packing
Das günstigste Angebot kann sich als das teuerste Projekt erweisen, wenn es zu Ausfallzeiten, Verschwendung oder ständigen Formatierungsproblemen führt.
TCO-Fragen, die Käufer oft vergessen zu stellen
● Welche Teile weisen den höchsten Verschleiß auf und in welchen Intervallen sollten sie üblicherweise ausgetauscht werden?
● Wie lange dauert ein tatsächlicher Personalwechsel mit einem eingearbeiteten Team?
● Wie hoch ist die zu erwartende Ausschussrate im Normalbetrieb?
● Was passiert, wenn eine wichtige Komponente ausfällt – egal ob sie lokal gelagert oder international versendet wurde?
Vertragsbedingungen, die Sie schützen
● Klare Liste der zu erbringenden Leistungen (Dokumente, Ersatzteile, Werkzeuge, Schulungen)
● Garantieumfang und -ausschlüsse
● Erwartungen an die Servicereaktion (auch wenn keine strikte Service-Level-Vereinbarung vorliegt)
● Meilensteinbasierte Zahlungen, die an konkrete Akzeptanzschritte gekoppelt sind
Globaler Einkauf ist in der Pharmaindustrie üblich. Wichtig ist nur, dass „global“ mehr bedeutet als nur „wir exportieren“.
Was zu bestätigen ist
● Unterstützung bei Versand- und Zolldokumentation
● Verpackungsstandards und Schadensmeldungsverfahren
● Ferninbetriebnahmemöglichkeit (bei eingeschränkter Reisetätigkeit)
● Verfügbarkeit lokaler Servicepartner (oder eines bewährten Reiseplans)
● Ersatzteillogistik (Lagerhaltungsplan oder schnelle Kanäle)
Wenn Interessensgruppen unterschiedlicher Meinung sind, kann eine einfache Bewertungsmatrix die Meinungen in eine Entscheidung umsetzen.
Hier ist ein einfaches Beispiel, das Sie anpassen können:
|
Kategorie |
Gewicht |
Wie „gut“ aussieht |
|
Maschinenanpassung (Ihre Dosierung + Leistung) |
25 % |
Nachweisbare Referenzen + klare Akzeptanzkriterien |
|
Dokumentationsbereitschaft |
20 % |
Beispiel-FAT + Handbücher + (falls erforderlich) IQ/OQ-Unterstützung |
|
Verarbeitungsqualität und Standards |
15% |
Transparente Bauteile/Materialien, einheitliche Montage |
|
Service & Ersatzteile |
20 % |
Klarer Reaktionsprozess, Ersatzteilplan, Schulungsumfang |
|
Kommerzielles und zeitliches Risiko |
20 % |
Reale Lieferzeiten, klarer Leistungsumfang, faire Garantiebedingungen |
Bewerten Sie jeden Lieferanten mit 1 bis 5 Punkten, multiplizieren Sie das Ergebnis mit dem Gewicht, und der „beste für Sie“ wird in der Regel schnell deutlich.
1) Wie viele Lieferanten sollte ich in die engere Auswahl nehmen?
Üblicherweise 3–5. Weniger als 3 begrenzen die Hebelwirkung; mehr als 5 erzeugen Störungen.
2) Benötige ich wirklich ein URS?
Ja – sogar eine kurze. Sie verhindert, dass Äpfel mit Birnen verglichen werden, und schützt Ihre Timeline.
3) Welche Dokumente sollte ich vor der Anzahlung anfordern?
Mindestens: Leistungsumfang, Anforderungen an Layout/Nutzung, FAT-Ablauf, Handbuchübersicht, Ersatzteilliste und Lieferzeitplan.
4) Was ist der Unterschied zwischen FAT und SAT?
Die Werksabnahmeprüfung (FAT) dient dem Nachweis der Leistungsfähigkeit beim Lieferanten; die Installations- und Funktionsprüfung (SAT) bestätigt die Installation und Funktion bei Ihnen vor Ort.
5) Wie kann ich die Einhaltung der GMP-Richtlinien durch einen Maschinenlieferanten beurteilen?
Achten Sie auf Nachweise: nachvollziehbare Bauprozesse, disziplinierte Dokumentation, Testprotokolle und ein validierungsbereiter Ansatz – abgestimmt auf die Märkte, in denen Sie verkaufen.
6) Ist es sicherer, eine komplette Produktlinie von einem einzigen Lieferanten zu beziehen?
Oftmals sicherer in Bezug auf Verantwortung und Inbetriebnahmegeschwindigkeit – aber nur, wenn sie eine wirkliche Integrationstiefe aufweisen.
7) Was ist, wenn ich Prüfprotokolle oder Funktionen für elektronische Aufzeichnungen benötige?
Sprechen Sie das Thema frühzeitig an und klären Sie, welche Erwartungen an elektronische Datensätze der Anbieter unterstützt und dokumentiert.
8) Welche Frage entlarvt schnell schwache Lieferanten?
„Zeigen Sie mir Ihr FAT-Protokoll und ein echtes Testprotokoll von einem ähnlichen Projekt.“

Welcher Lieferant ist also der beste für Sie? Die Antwort ist meist derjenige, der diese Prüfungen am unkompliziertesten besteht: klar definierter Leistungsumfang, nachgewiesene Maschinenkompatibilität, lückenlose Dokumentation, systematische Tests und ein zuverlässiges Servicemodell. Wenn Sie so vorgehen, geht es bei der Auswahl eines Herstellers von Pharmamaschinen weniger um Verkaufsgespräche, sondern vielmehr um Fakten, Ergebnisse und langfristige Verfügbarkeit.
2.Europäische Kommission: EudraLex Band 4 (EU-GMP-Leitlinien, inkl. Anhang 15).
3.FDA: Teil 11 — Elektronische Aufzeichnungen; Elektronische Signaturen (Geltungsbereich und Anwendung).
4.PIC/S: Leitfaden für die gute Herstellungspraxis von Arzneimitteln (PE 009). ( picscheme.org )